
研究背景

短肠综合征(SBS)是由于失去了大部分肠道导致的一种以腹泻、脂肪泻、腹痛、电解质紊乱、脱水和营养不良为特征的致残性疾病。残余肠道具有适应能力,以补偿吸收表面积的减少,这主要与胰高血糖素样肽-2(GLP-2)有关。GLP-2是一种33个氨基酸的多肽,由胰高血糖素经翻译后加工而成。
目前,用于补偿肠道缩短的激素有限,大多数SBS患者需要受药物治疗。人类生长激素、促生长素和左旋谷氨酰胺已被批准用于SBS的短期治疗,但疗效有限。替度鲁肽被批准用于长期治疗SBS的药物,该药物是GLP-2的类似物,与GLP-2一样,替度鲁肽通过与肠道组织中的GLP-2受体胞外结构域(ECD-GLP2R)结合发挥药理作用。ECD-GLP2R的三维(3D)结构尚未确定,因此它与激动剂/拮抗剂的相互作用模式也不清楚。利用配体-受体复合物的三维(3D)结构来可以更好地理解它们在原子水平上的相互作用模式,进而设计出具有更好生物活性的新配体。
研究方法
参照文献中的研究方法,本文使用MaXFlow平台分子模拟相关功能组件完成所需的各项计算任务。采用蛋白-多肽对接和分子动力学(MD)模拟相结合的策略揭示了ECD-GLP2R和替度鲁肽之间的相互作用机制。首先,利用同源建模构建并优化了ECD-GLP2R的三维结构,以及肽段构建方法构建出替度鲁肽的三维结构。然后,通过蛋白-肽对接预测了ECD-GLP2R与替度鲁肽结合的初始姿势,通过计算RMSD、RMSF、回旋半径、氢键数量、二级结构和系统模拟中的总能量以及分子力学/泊松-波尔兹曼(广义波恩)表面积(MM/PB(GB)SA)并进行了评估。
1、数据准备
GLP-2R蛋白:从UniProt获取GLP2R_HUMAN的序列信息,将其保存为.fasta格式。
替度鲁肽:序列信息 HGDGSFSDEMNTILDNLAARDFINWLIQTKITD
2、模型构建
在MaXFlow平台采用同源建模的方法构建出ECD-GLP2R的三维结构。
第一步序列识别:
读取目标蛋白序列信息
第二步模板查找:
文献中使用的模板(PDB ID:6GB1),在这里选择序列评分更高、相似性更高的5YQZ作为模板结构。
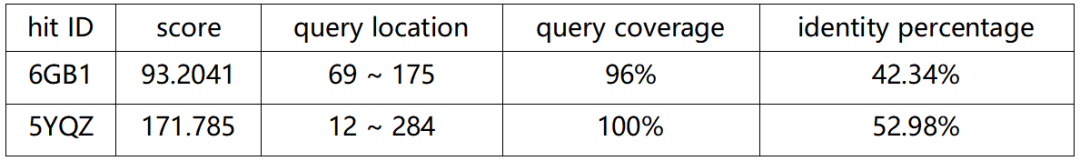
第三步参数设置:
选择Amber力场优化建模后的蛋白结构,并提供拉式构象图(Ramachandran plot)评估同源建模后模型的质量。
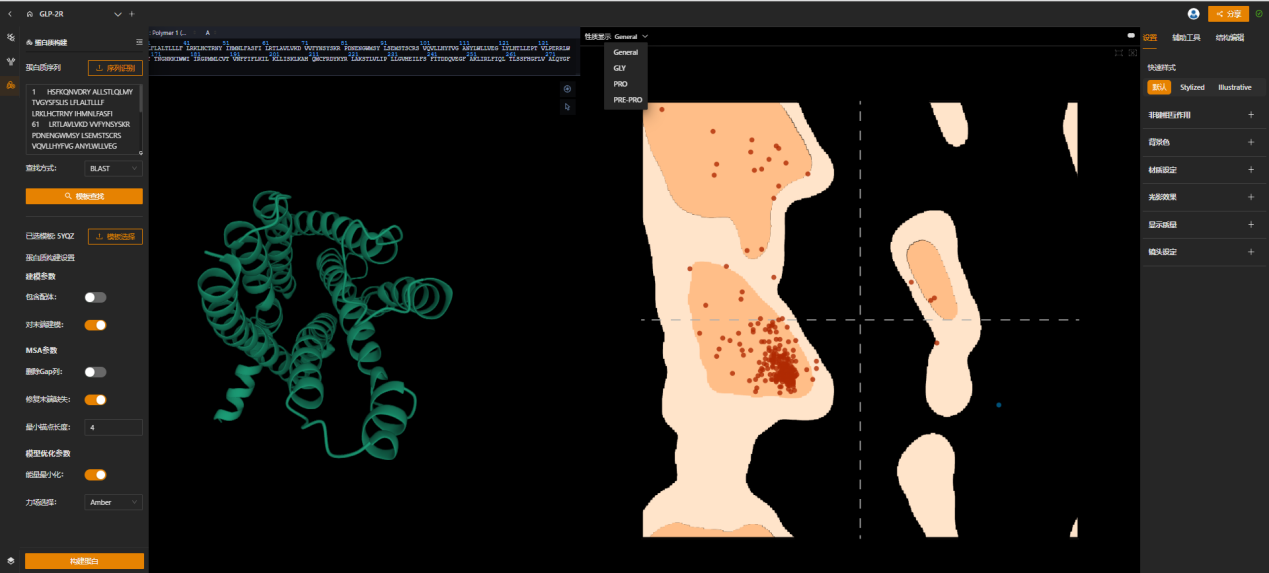
在MaXFlow平台进入肽段构建,输入序列选择相应的二级结构类型即可构建出替度鲁肽三维模型。

3、替度鲁肽-GLP-2R对接
多肽-蛋白对接
该方法可用于不超过20 个氨基酸的多肽与受体蛋白对接,能处理不同长度和类型的多肽,包括线性、环状(包括通过主链肽键、侧链肽键或侧链二硫键不同环化方式环化的肽)、含有非天然氨基酸或修饰的多肽。
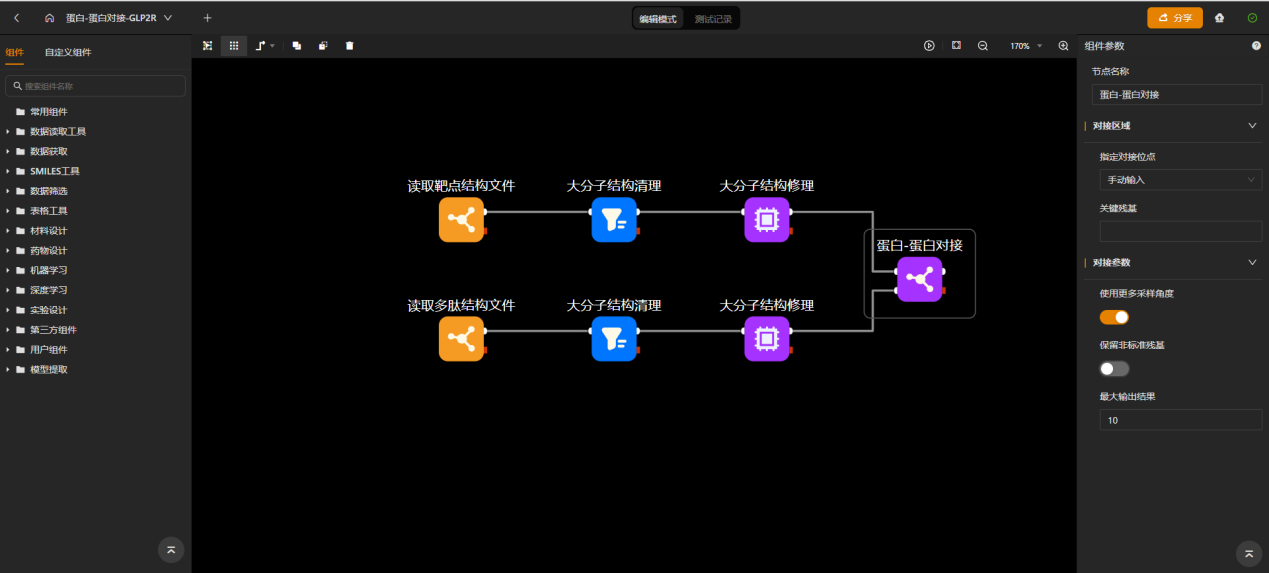
分别输入上述已构建好的结构,并设置对接位点。
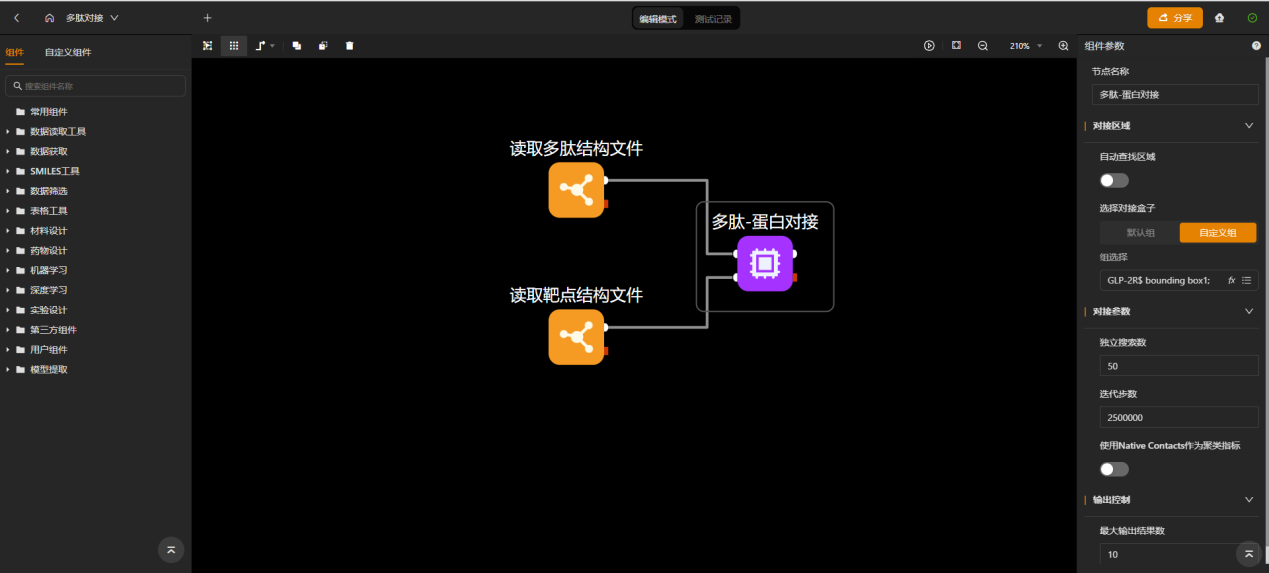
如果该受体蛋白和多肽结构从其他数据库中下载,需要添加大分子结构清理和大分子结构修理,去除掉影响对接的小分子。如果对接位点未知,可采用自动查找区域的方法,该方法根据疏水性以及氢键供体受体等性质预测高亲和力位点。
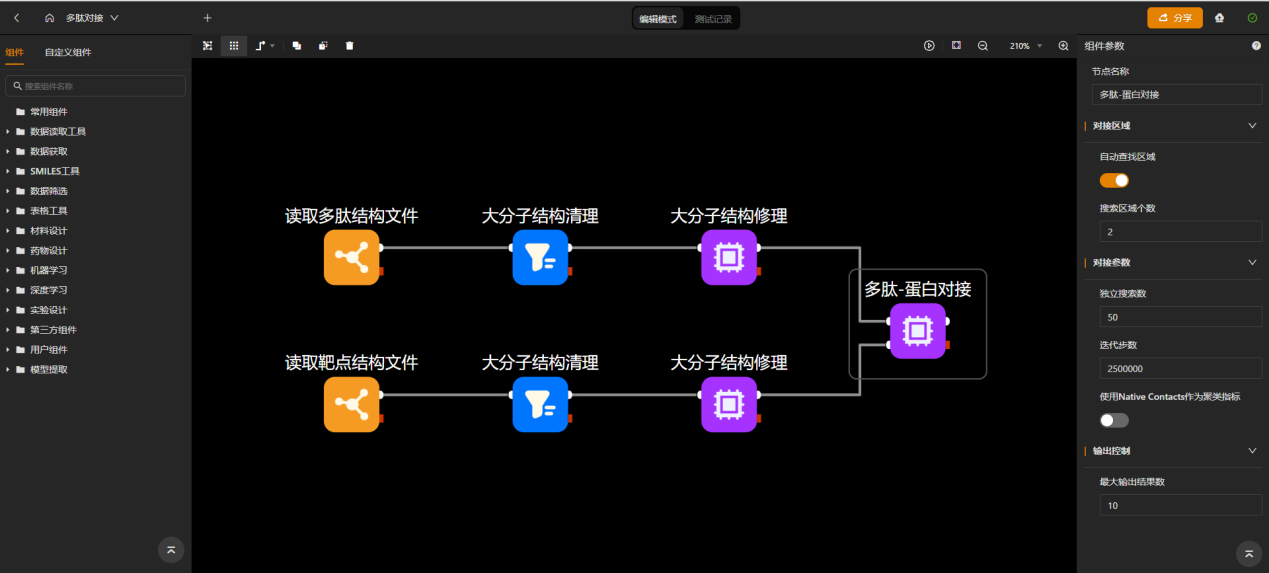
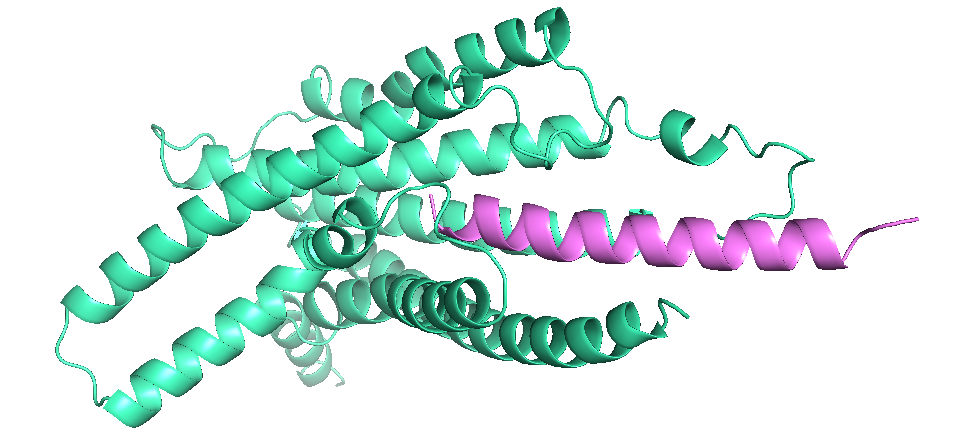
图丨替度鲁肽-GLP-2复合物结构
蛋白-蛋白对接
对于序列较多的多肽,可以采用蛋白-蛋白对接方法,手动输入对接位点序列信息。
4、替度鲁肽与GLP-2R复合物的分子动力学模拟
选择上述对接评分最高且能结合在活性位点的复合物模型作为分子动力学模拟的初始结构,本次模拟采用了曙光DCU加速计算,平衡模拟100 ns,并分析了短程库仑相互作用和短程范德华相互作用、RMSD、RMSF、回旋半径、氢键分析、二级结构分析、盐桥分析、π-π堆积分析以及,并对分子力学/泊松-波尔兹曼(广义波恩)表面积(MM/PB(GB)SA)进行了评估。
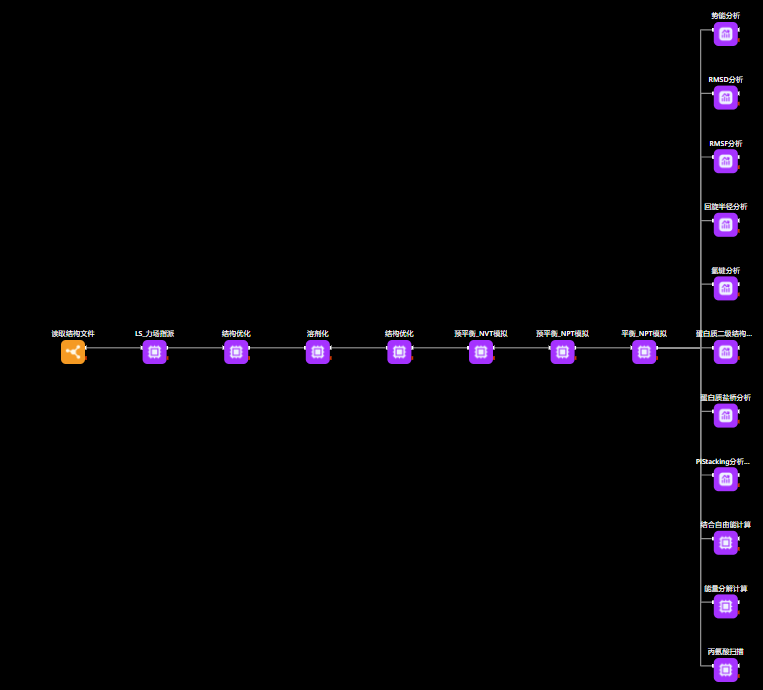
图丨分子动力学模拟工作流
待模拟完成后,对该复合物的动力学轨迹进行分析,可以做结构稳定性分析、热稳定性分析、构象转变分析、非键相互作用分析(如氢键、π-π堆积、盐桥)、结合自由能及能量分解、丙氨酸扫描热点残基分析等。
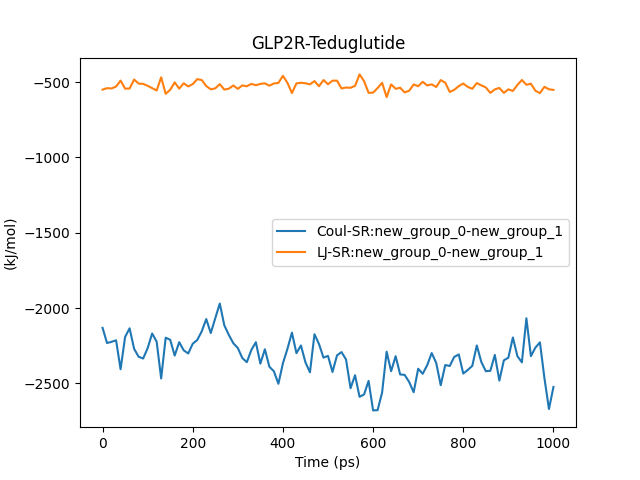
图丨势能分析:短程库仑相互作用和短程范德华相互作用
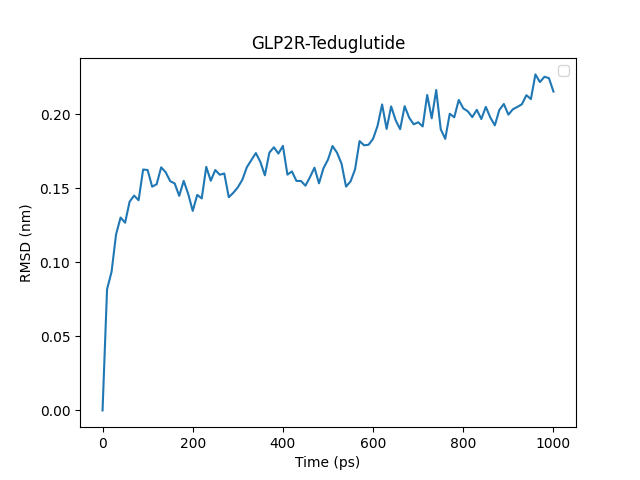
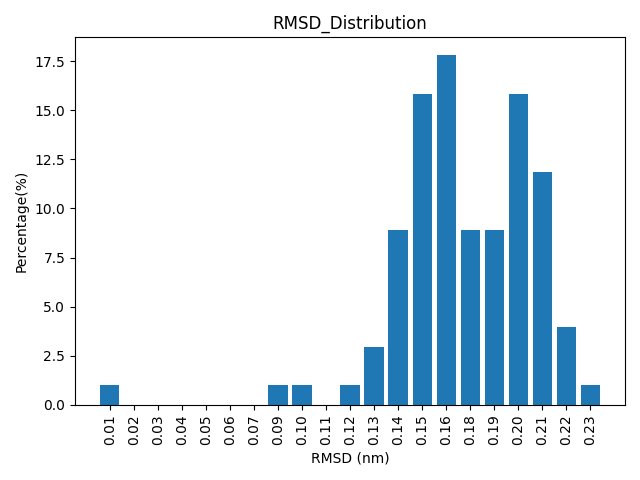
图丨RMSD值及RMSD分布分析
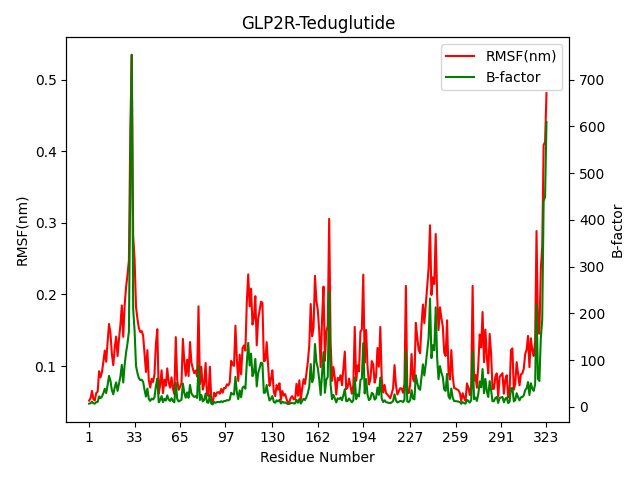
图丨RMSF及B-factor分析
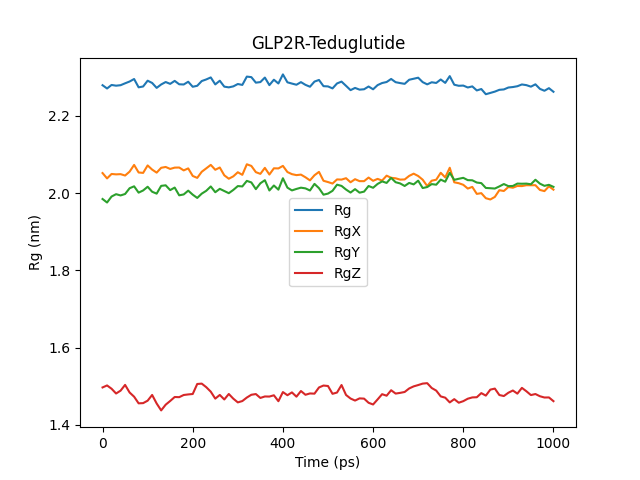
图丨回旋半径分析
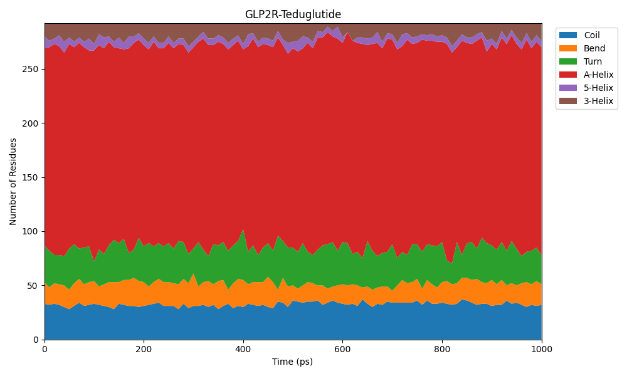
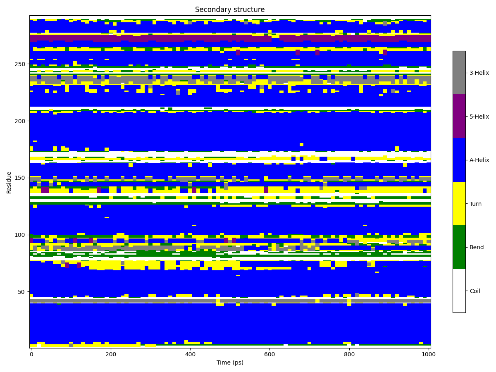
图丨二级结构分析
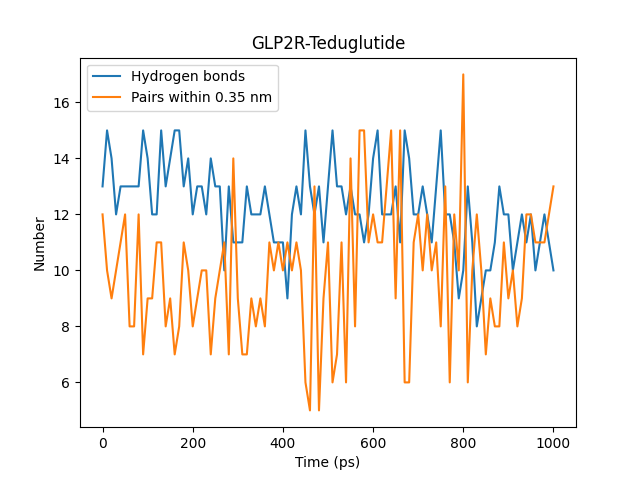
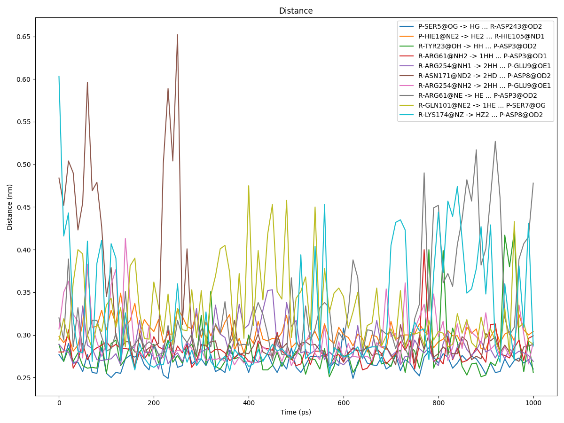
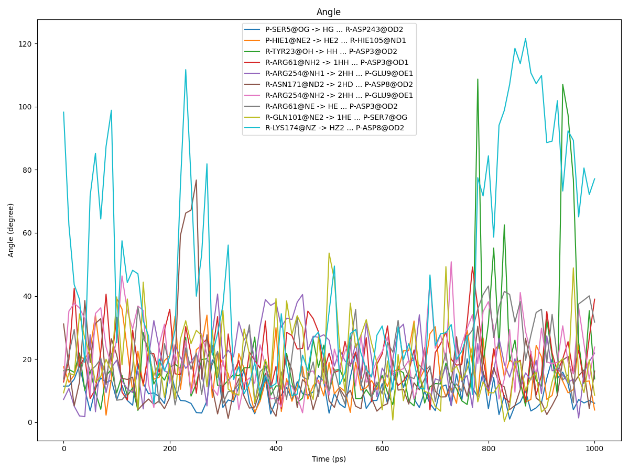
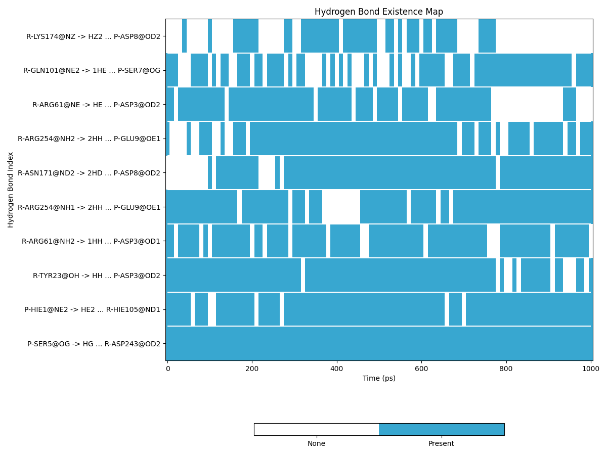
图丨氢键分析
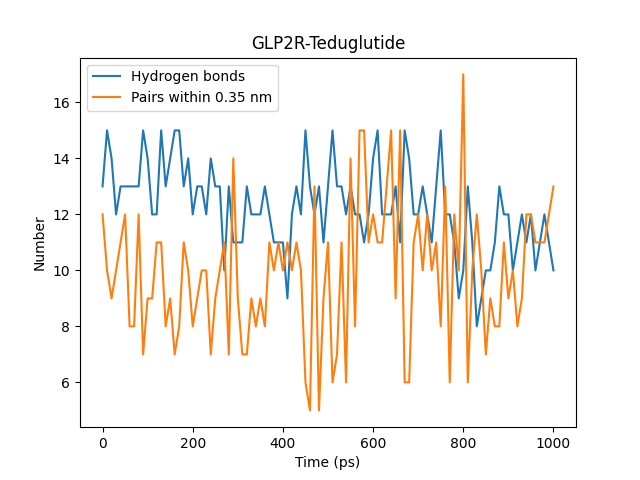
图丨盐桥分析
表丨结合自由能分析
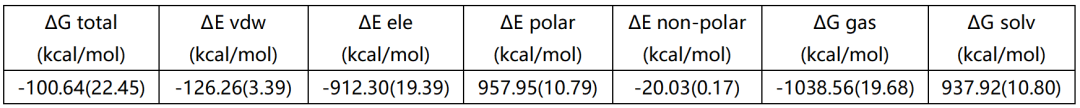
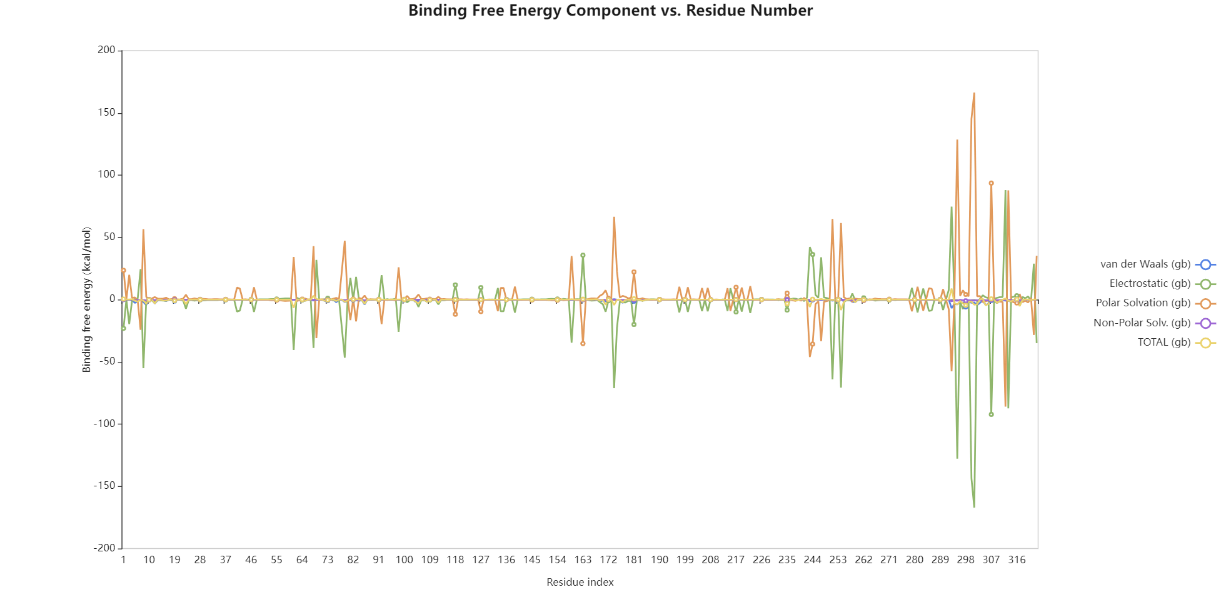
图丨能量分解
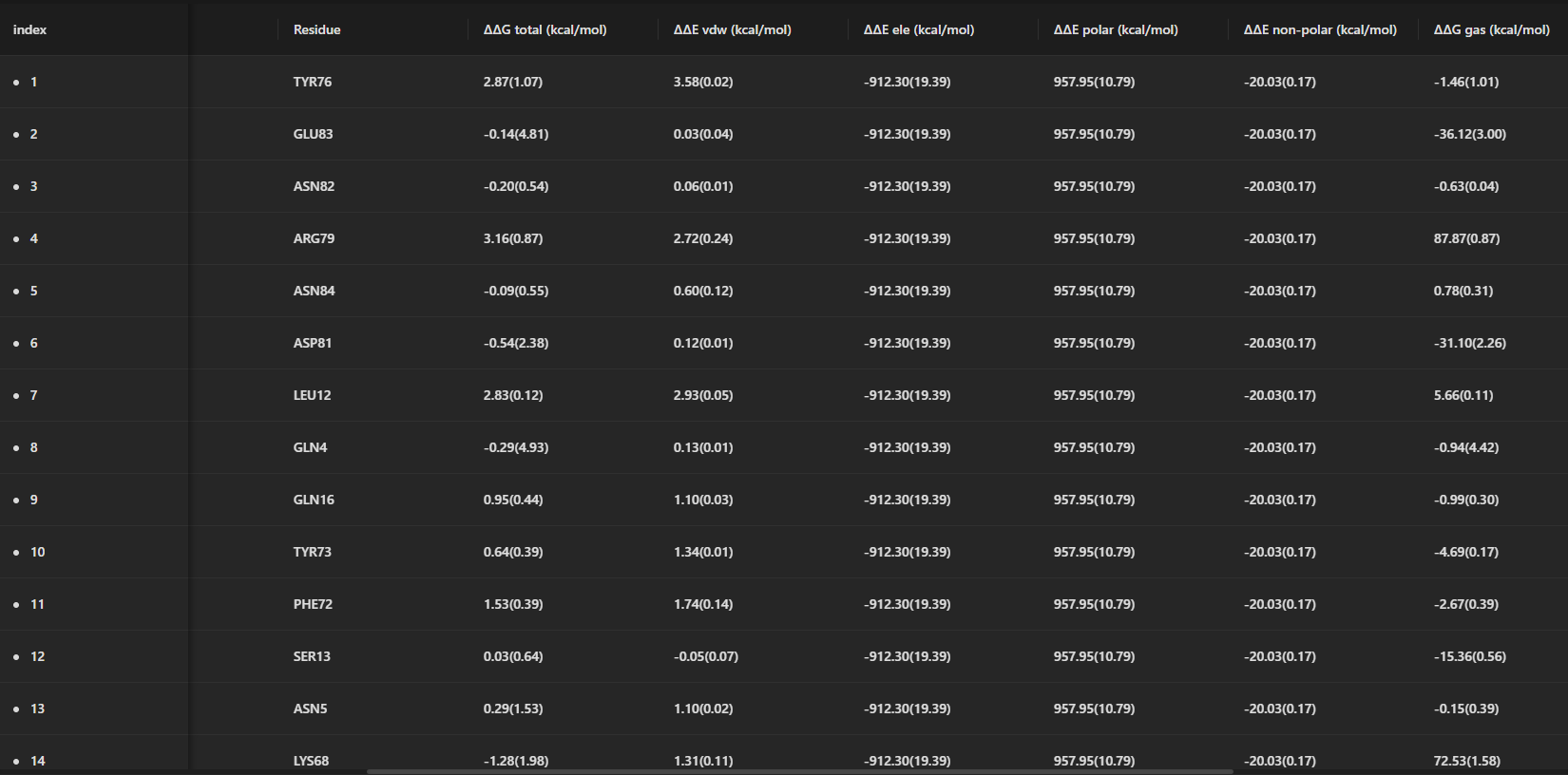
图丨丙氨酸扫描分析
总结
本文使用MaXFlow人工智能和分子模拟平台,以胰高血糖素样肽-2受体胞外结构域和替度鲁肽的序列为输入,采用同源建模的方法构建了GLP-2R的三维结构,同时构建了多肽的结构。之后以这两个结构为基础,采用多肽-蛋白对接功能,选择高质量的对接结果,进行分子动力学模拟,探究两者之间的相互作用模式,进而设计出具有更好生物活性的新配体。
MaXFlow是一款强大的计算化学工具,它可以应用于多肽药物的设计和优化过程中。在理论层面上,MaXFlow能够利用分子模拟、分子力学以及机器学习等方法来预测和分析多肽的三维结构、稳定性和功能活性。通过这些先进的计算技术,研究人员可以模拟多肽药物与受体或其他生物大分子之间的动态相互作用过程,揭示关键的氢键网络、疏水作用等因素对药物活性的影响,从而指导实验研究并加速药物开发进程。
申请产品试用
