
基于异氧氟烷醇和N-isobutyl-N-(4-chloro-benzyl)-4-chloro-2-pentenamide的结构,通过连接它们的药效团,设计了一系列N-benzyl-5-cyclopropyl-isoxazole-4-carboxamides(即多靶点药物设计策略)。由5-环丙基异恶唑-4-羧酸和取代苄胺合成了27个N-benzyl-5-cyclopropyl-isoxazole-4-carboxamides,其结构经核磁共振和质谱确证。室内生物测定表明,10 mg/L的I-26对马齿苋和布丁香麻的抑制率为100%,优于阳性对照丁草胺(对这两种杂草的抑制率均为50%)。在培养皿中观察到IFT有很强的生长抑制作用,但没有观察到典型的漂白现象。I-05在出苗后表现出良好的除草活性,除草速度为150g/ha,处理后的杂草叶片出现漂白症状。I-05处理的莱茵衣藻的漂白效果可以通过添加均一酸来逆转。酶生物测定表明,I-05不抑制4-羟基苯丙酮酸双加氧酶(HPPD)活性,而I-05的异恶唑开环产物II-05对HPPD有抑制作用,EC50值为1.05μM,与美索曲酮相似(EC50值为1.35μM)。关于观察到的除草症状的详细讨论在结果和讨论部分提供。本研究为多靶点药物设计策略在农化研究中的应用提供了概念验证基础。
分子对接(molecular docking)是基于结构药物设计的核心模拟手段,依据受体与配体作用时的几何匹配和能量匹配过程,模拟受体-配体相互作用,预测两者间最佳的结合模式和结合亲和力。采用分子对接模拟技术,科研人员可以进行基于结构的药物虚拟筛选,药物分子的结构改造,药靶相互作用的机理研究等工作,从而大大提高实验效率。在BIOVIA Discovery Studio这一分子模拟的综合平台中,共有四种对接程序,包含Libdock、CDOCKER、FlexibleDocking,这三种对接算法各有优势,能够满足广大科研工作者的多种应用需求,为其提供配体受体间相互识别的“利器”。
ref:J. Agric. Food Chem;IF=4.192
链接:https://dx.doi.org/10.1021/acs.jafc.0c03582
4-羟基苯基丙酮酸双加氧酶(HPPD)是植物体内质体醌生物合成途径中的一个重要酶,通过阻断HPPD抑制质体醌的生物合成导致除草活性和独特的漂白症状。1997年,HPPD被确定为三酮类化合物的靶点。近年来,HPPD抑制剂的发现取得了很大进展,三酮类、异恶唑类和吡唑类化合物得到了广泛的应用。目前,新型HPPD抑制剂的发现引起了除草剂行业的广泛关注。异氟草醚(IFT)是一种前驱HPPD除草剂,用于防除玉米和甘蔗的阔叶杂草和禾本科杂草。尽管IFT是一种高效除草剂,但在实际应用中,IFT对杂草的光谱和对作物的选择性都不够好。为了克服这些缺点,IFT通常与氟草净、克隆尼芬或阿特拉津混合使用,以提高其对杂草的除草活性,而环丙磺酰胺则被用作制剂中的安全剂。为了克服这些缺点,有必要开发新的化学。多靶点药物设计是医药领域的一种新策略,已有多个成功的实例报道。然而,这一策略在农化研究中鲜有报道。对于多靶点药物设计可以实现不同的方法。在这些方法中,将药效团与连接子或不与连接子合并是一种公认的方法。该方法要求两种先导化合物具有相似的化学结构和生物活性。IFT不抑制植物中的HPPD。它的活性来自开环转化的产物(即从异恶唑到二酮腈或DKN)。这种开环转化是一种快速的非酶水解,在植物和土壤中都会发生。DKN的螯合性1,3-二酮负责与HPPD的活性位点结合。因此,异恶唑-4-羰基被认为是IFT的药效团。本设计采用的另一种含铅除草剂是库麦化学有限公司报道的一种光依赖型酰胺类除草剂N-isobutyl-N-(4-chlorobenzyl)-4-chloro-2-pentenamide,它可以通过抑制细胞分裂而有效地防治藜草。根据其结构,羰基苄胺被认为比柔性侧链更重要。因此,该部分被认为是该先导除草剂的药效团。本研究的目的是采用多靶点药物设计策略,将IFT的药效团(即异恶唑-4-羰基)和Nisobutyl-N-(4-chloro-benzyl)-4-chloro-2-pentenamide的药效团(即羰基苄胺)合并。由于两个药效团共用一个共同的羰基,所以采用了不带接头的合并,形成了新型的羧胺类化合物。设计合成了27个N-benzyl-5-cyclopropylisoxazole-4-carboxamides,其结构经核磁共振和质谱确证,并通过培养皿实验和温室盆栽实验对其除草活性进行了评价。发现了活性化合物(如I-05、I-24和I-26),并对某些化合物(如I-05和I-24)进行了藻类和出苗后盆栽试验,观察到典型的HPPD抑制漂白现象。这些活性化合物可作为除草先导进行进一步优化。
作物HPPD和杂草HPPD(如玉米HPPD和拟南芥HPPD或AtHPPD)之间可能存在差异,这导致了除草剂在作物和杂草之间的选择性。我们的目的是看看HPPD是否可以作为标题化合物的靶标之一(即是否HPPD),以及是否可以被标题化合物和阳性对照-商品除草剂美索曲酮(即并列比较)所抑制。我们实验室可以很容易地制备玉米HPPD,但AtHPPD在我们实验室并不容易获得,因此玉米HPPD被用于这一目的。如表1所示,II-05、II-24和美索曲酮对HPPD有抑制作用,其IC50值分别为1.05、1.28和1.34μM。而I-05和I-24对HPPD无抑制作用。结合I-05不抑制HPPD,II-05抑制HPPD,藻类漂白和出苗后漂白现象等信息,表明I-05在体内(如藻类和植物)可以缓慢转移到II-05,因此I-05和其他活性化合物(如I-24)可能是前药。对于IFT来说,异恶唑的开环转化是一种快速的非酶水解,在植物和土壤中都会发生。快速水解可能来自位于两个环之间的吸电子羰基的强烈作用,它可以在三酮和酮烯醇间形成一个非常稳定的平衡。对于标题化合物(如I-05和I-24),由于较强的电负性氮,羧酰胺基团中羰基的吸电子效应变得较弱。因此,标题化合物的异恶唑环水解可能会变得非常缓慢,或者可能由特殊的代谢酶发生,这可以解释为什么在藻类试验和出苗后的盆栽试验中可以观察到漂白症状,而在培养皿试验中没有观察到漂白症状。
通过分子对接方法研究了II-05和II-24的活性实体以及I-05和I-24与HPPD的相互作用。如图1所示,II-05和II-24与FeII形成双齿相互作用,苯环可以与Phe360和Phe403形成π−π相互作用。II-05的CN基团与Asn261的氨基形成氢键,这可能是导致除草活性增加的原因。通过比较π−π相互作用的距离,我们发现II-05和Phe360的苯环距离大致等于II-24的苯环距离,而II-05和Phe403的苯环距离(3.7埃)小于II-24的苯环距离(4.3埃)。距离的增加可能是I-05除草活性略强于I-24的原因。在DS的CDOCKER模块中,使用−CDOCKER相互作用能来评价对接效果。得分越高,表明药物与受体之间的结合越好。米索曲酮、II-05和II-24的-CDOCKER_INTERACTION_ENERGY分别为55.98kcal/mol、49.78 kcal/mol和38.08 kcal/mol。II-05的得分显著高于II-24。这可能是由于II-05比II-24多一个氢键相互作用。I-05和I-24出苗后除草活性的差异也与分子对接结果一致。
综上所述,本论文基于多靶点药物设计的策略,合成了一系列N-苄基-5-环丙基异恶唑-4-羧酰胺类化合物。通过合并药效团的概念,将HPPD的药效团和酰胺类除草剂结合到标题化合物的结构中。标题化合物可以很容易地以良好到优异的产率制备。在培养皿试验中,部分化合物对杂草表现出较强的抑制作用,表现出与酰胺类除草剂相似的症状。I-05具有良好的出苗后除草活性,可作为HPPD抑制剂的前药。虽然与新推出的除草剂相比,其活性相对较低,但本研究为新除草剂的发现提供了一个潜在的多靶点先导化合物。

表1 受试化合物对HPPD的抑制作用
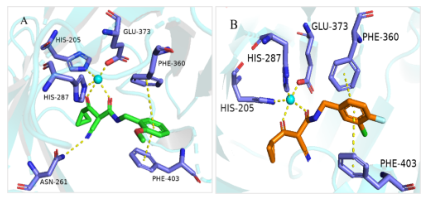
图1:II-05和II-24与AtHPPD的结合模式。A)II-05与AtHPPD.II05的结合模式。(B)II-24与AtHPPD的结合方式
为什么选择 BIOVIA Discovery Studio?
1. BIOVIA Discovery Studio 中共有四种对接程序,这四种对接算法各有优势,能够满足广大科研工作者的多种应用需求;
2. BIOVIA Discovery Studio 中有多种对接结果的评价分析手段,包括2D/3D相互作用图分析(可以分析氢键、疏水作用、卤键等多种非键作用类型)、结合口袋表面分析、氢键热图、多种打分函数、结合能的计算等;
3. BIOVIA Discovery Studio 应用广泛,操作简便,图形化界面十分友好,结果易于分析。