
当前电子实验记录本(ELN)在国内越来越普及,自2020年7月NMPA颁布了《药品记录与数据管理要求(试行)》给高度受监管的制药行业吃了一颗定心丸,法规中明确了电子记录的相关要求,承认了电子记录与纸质记录具有同等效力!
图 | 《药品记录与数据管理要求(试行)》
相信有大家会有这样的困扰,上线电子实验记录本时,在合规性要求方面,究竟需要关注哪些问题?
01 权限与密码管理
电子实验记录本ELN须具备用户权限设置与分配功能,并能够对权限修改痕迹进行记录与查询;可根据使用者职责范围进行不同角色用户权限的分配,与此同时,通过账号密码管理策略,严格控制数据访问及操作,以确保数据的安全性及有效性。电子签名,应当符合《中华人民共和国电子签名法》的相关规定。
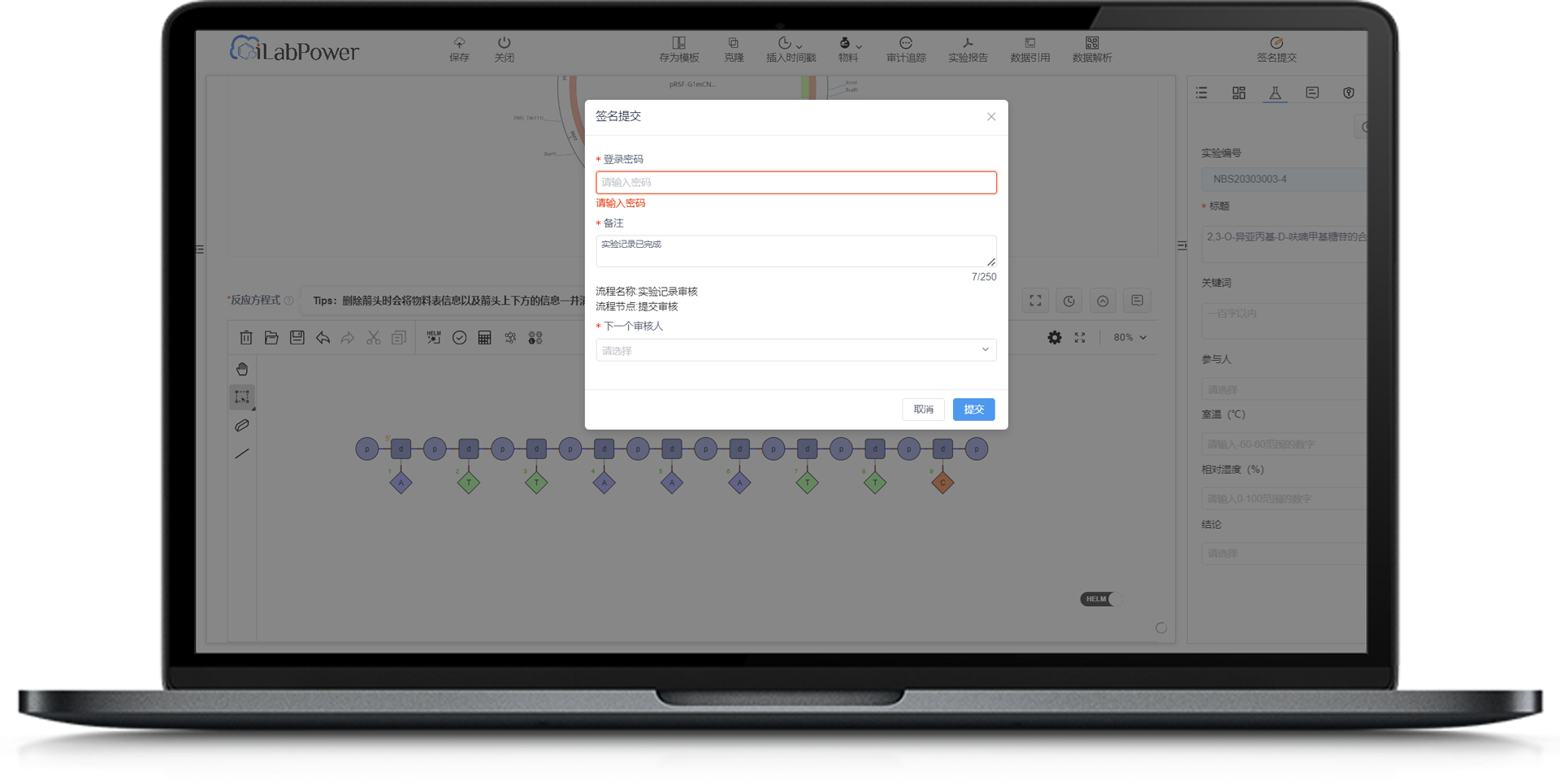
iLab Power ELN界面 | 电子签名界面
02 审计追踪
电子实验记录本ELN的审计追踪功能须包括:
1) 电子实验记录创建、审核和修改的审计追踪
电子实验记录本,应该可以实现不同审批状态下的实验记录修改,并通过审计追踪功能记录修改人、修改时间、修改的新值、旧及修改理由,确保数据的真实、准确、完整和可追溯。
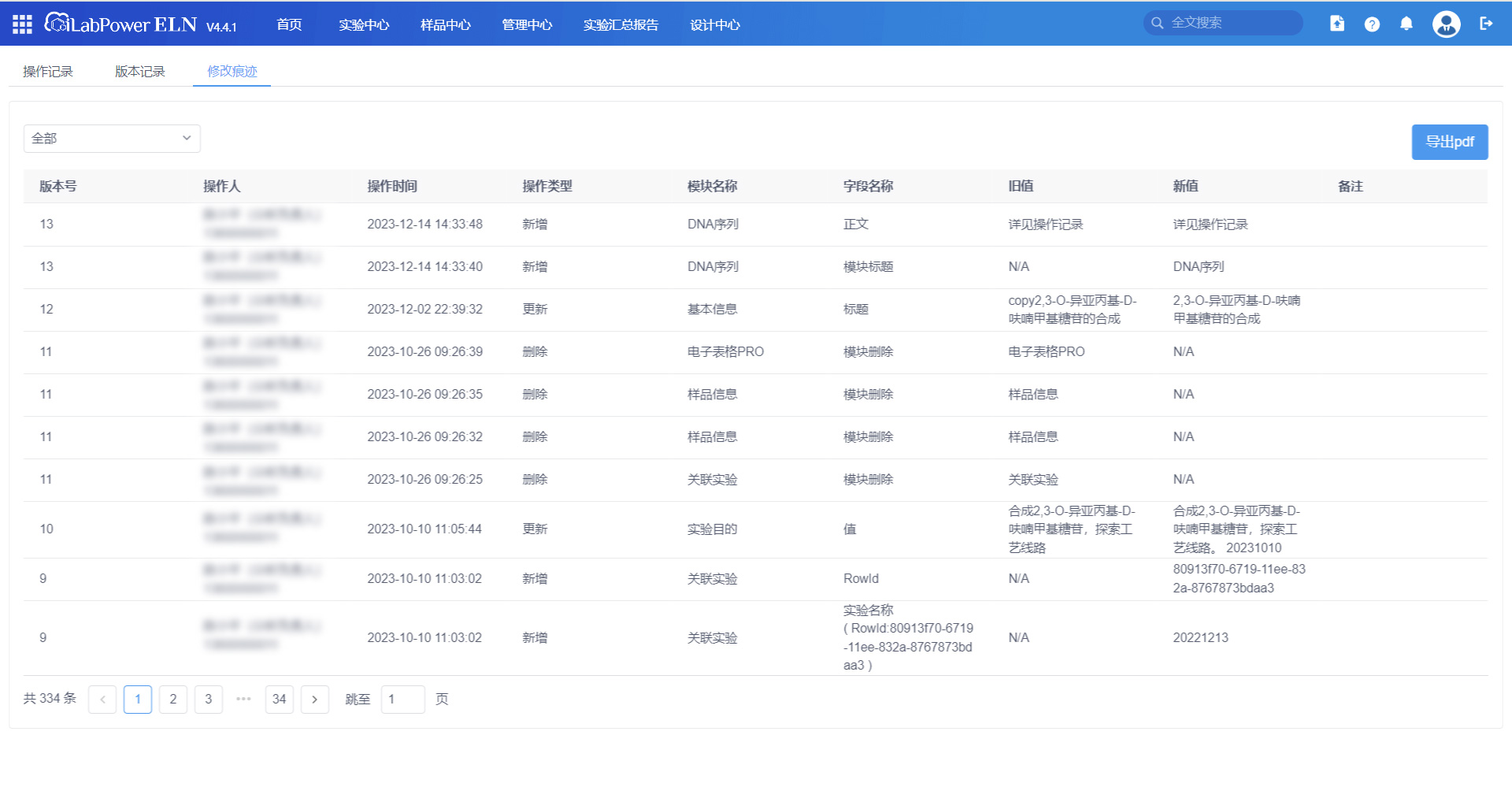
电子记录修改痕迹-审计追踪
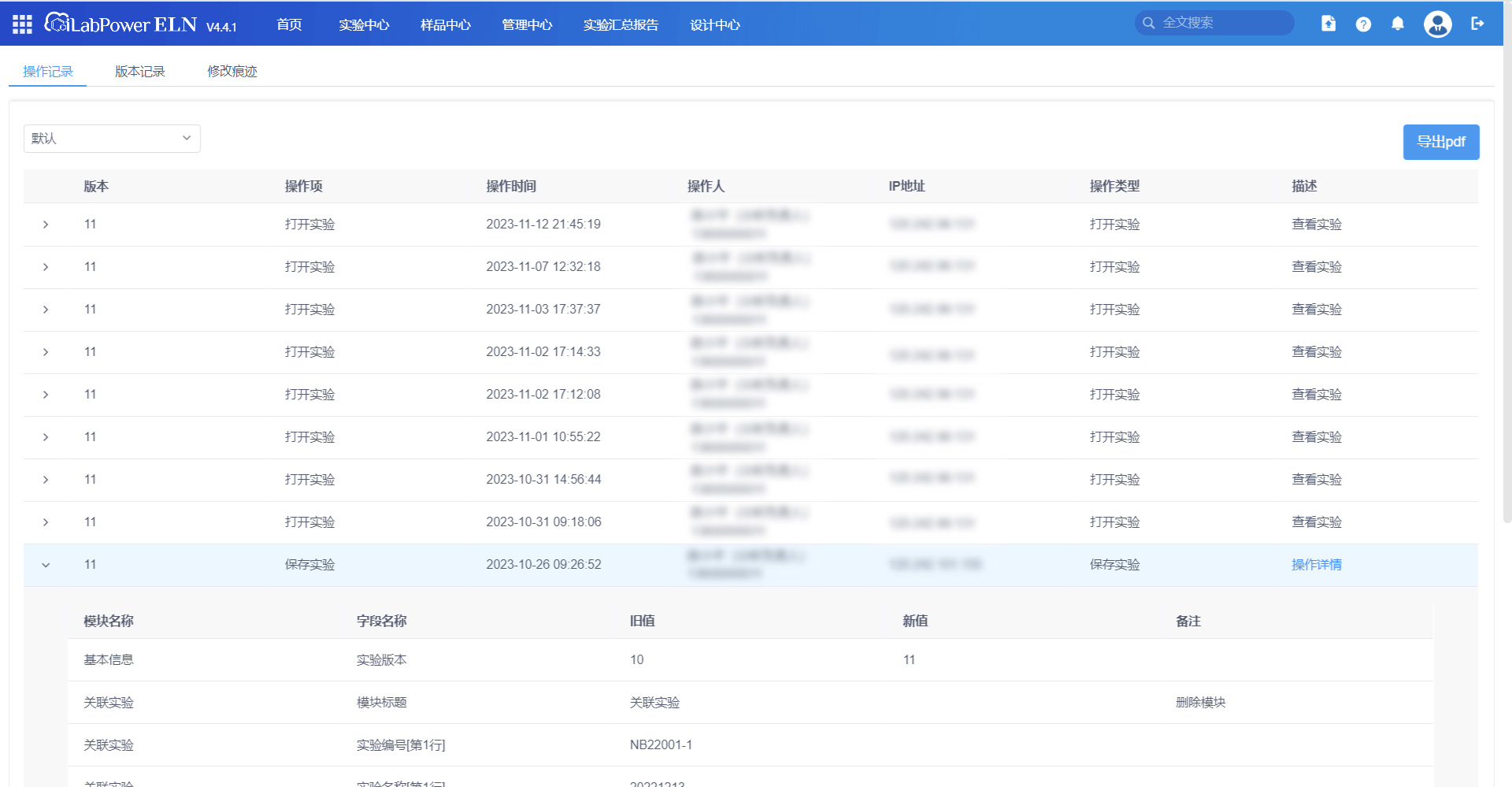
操作记录-审计追踪
2) 权限配置的审计追踪
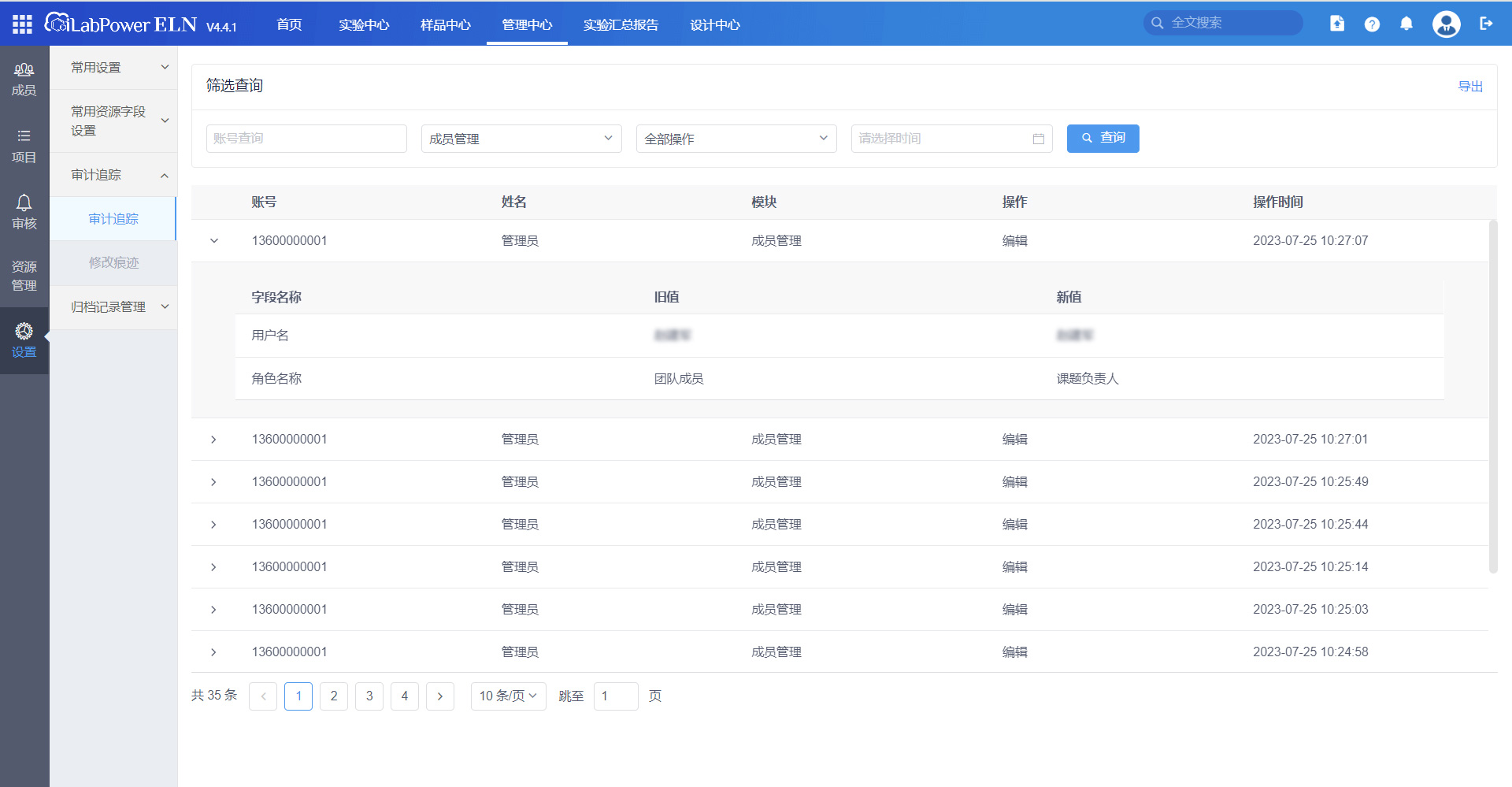
成员管理-审计追踪
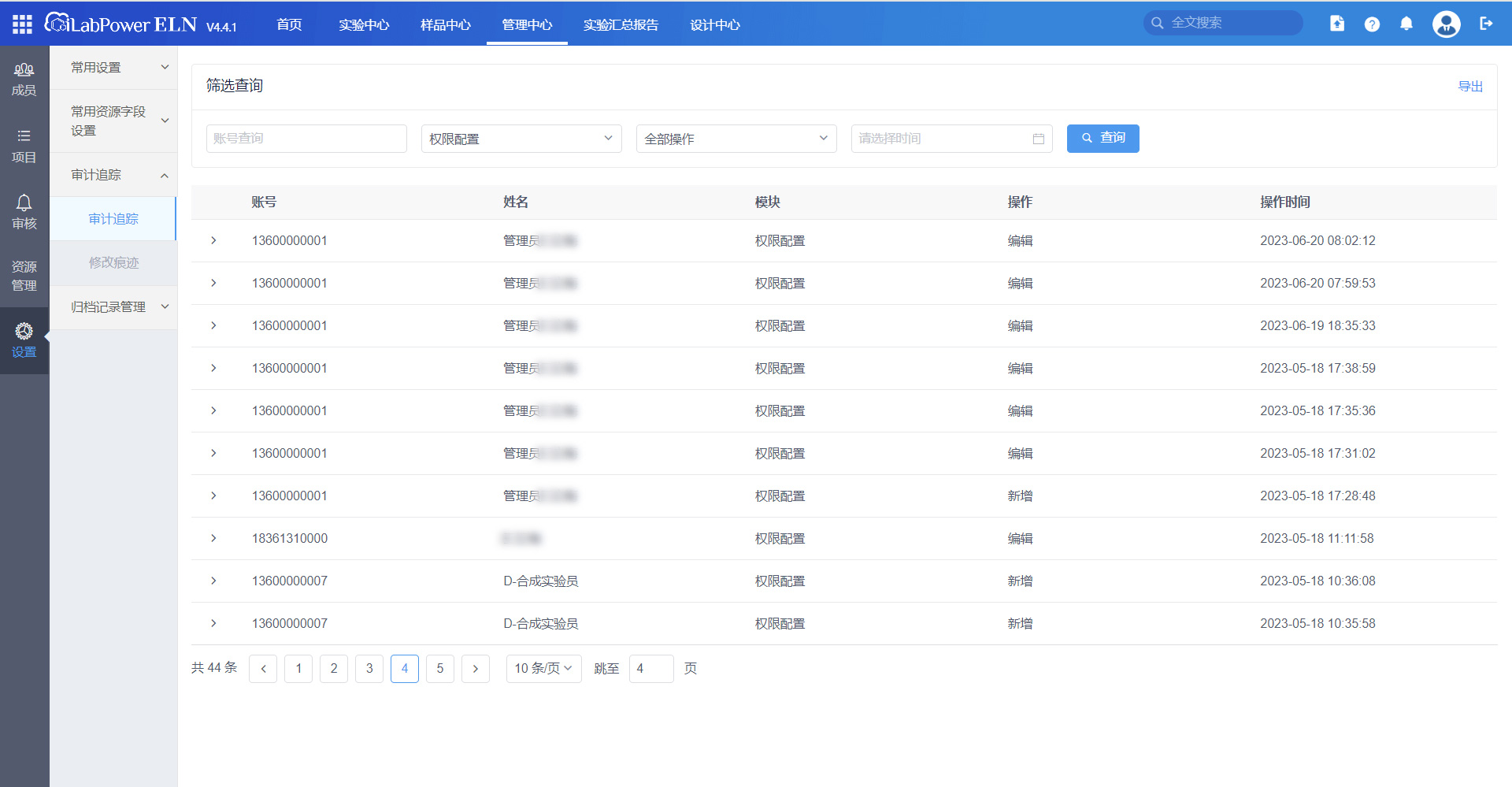
权限配置-审计追踪
03 数据复核
电子实验记录本ELN能够满足数据复核操作的执行,实现人工复核及电子复核,确保数据录入的准确性和处理正确性。
除满足上述功能要求外,对于GxP以及相关法规中明确规定计算机化系统在正式上线使用前,还须采用基于科学和风险的方法有效实施计算机化系统验证,以此降低受监管企业引入电子实验记录本的合规风险。
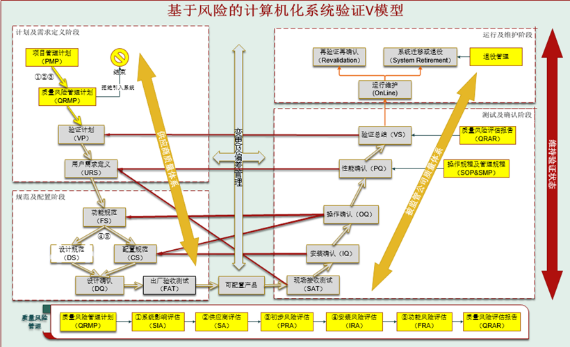
经过十余年的科技发展与行业法规更新,计算机化系统也随之发生了翻天覆地的升级,目前越来越多的应用程序采用基于云的SaaS服务方式。如何积极拥抱云,充分利用云带来的益处也日渐成为受监管公司关注的重点。
云服务目前在一些法规指南中也出现了它的身影。例如在新修订的GAMP5第二版中也充分体现了这一点。第二版附录M1-验证计划中的角色和职责一节中提到了云供应商提供承担系统规范、验证活动和操作控制的责任,除此以外,在其他章节如生命周期阶段、供应商活动、风险管理等中都有提及云计算服务实施和管理的指导意见;
在欧盟新版GMP附录11计算机化系统概念文件中提及云系统/云服务是被接受的;还明确了云供应商的职责;
在2023版的中国药品GMP指南厂房设施与设备一书中也提及了对于应用云服务的技术要求。指南主要从云计算服务模式类型、云技术要求、实施云计算部署指导意见等内容进行了说明。
此外,GAMP5第二版中还强调了供应商的重要性,鼓励受监管公司最大限度地利用供应商的人员、知识、经验和能力。如果供应商在发布产品前,已按照GxP相关法规要求执行了验证,那么就可以在保证合规性相关风险可控的前提下大幅加快系统上线进度、降低成本。
