

Pinnacle 21 是为准备临床试验数据进行监管提交软件领域的全球领导者。全球 25 家最大的生物制药公司中有 22 家信任 Pinnacle 21 Enterprise。因其CDISC标准依从性和易用性,Pinnacle 21 Enterprise被美国 FDA 、日本 PMDA以及中国NMPA信任,用于审查递交的数据质量。
您也可以根据数据集的监管机构拒绝标准来检视您的数据集,从而提前修复问题,降低风险并加快审查过程。
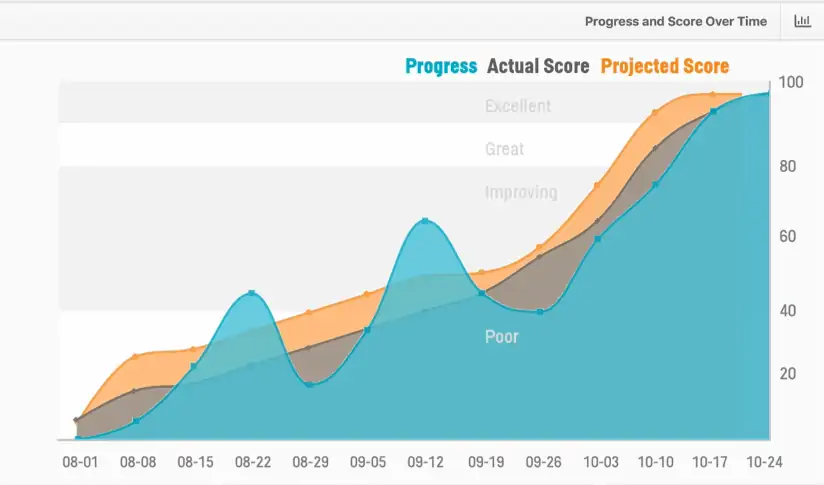
使用仪表板和评分算法来监控提交数据的准备进度。
使用清晰的前后视图跟踪多次数据集验证之间的改变。
通过我们预先构建的图形报表深入挖掘您的数据组成,从而发现与标准的不一致。
您的数据适应度得分是多少?
软件会检查您的数据是否符合目标监管机构的业务实施细则,是否符合 CDISC 标准、受控术语以及 MedDRA 和 WHODrug 等编码字典的要求。对检查出的问题提供参考意见和“Fix Tips”,以便您的数据可以安心递交。

数据质量的持续改善
在试验进行期间解决数据可能的质量问题,并尽可能早的去验证数据,从而最大限度地降低监管延误的风险。赞助商可以与合作伙伴和供应商共同访问Pinnacle 21 Enterprise平台,我们的嵌入式反馈循环可以帮助您和您的合作者不断改善数据质量。此外,您还可以将您的自定义标准、术语和业务规则上传到我们的验证器中,以查看哪些符合 CDISC 以及哪些需要改进。确保每个人的可交付成果永久合规并随时可以提交。
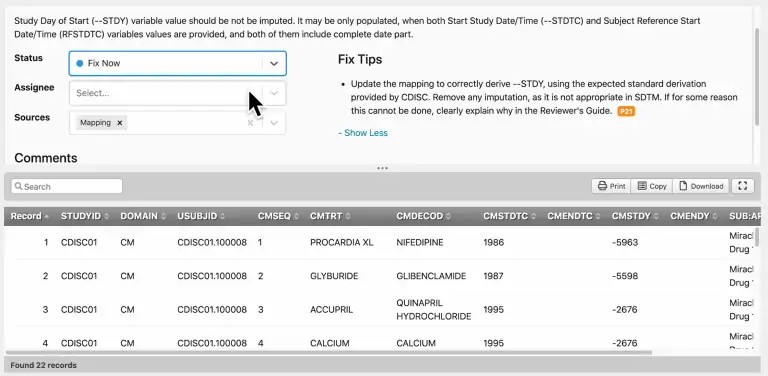
通过无缝问题管理维护单一事实来源
与开发人员和外部供应商合作,将分散团队整合起来协同解决问题并使数据集标准化。比如通过批量操作和自动化快速批处理;通过预先设置的状态和来源,为验证问题设置自定义默认值;引入您自己的工作流程,我们的平台支持任何复杂的用例。不同分类使用同一的标签和过滤器,您可以通过编程来批量解决一系列问题、分配给其他协作用户或让它们随着时间的推移而解决。
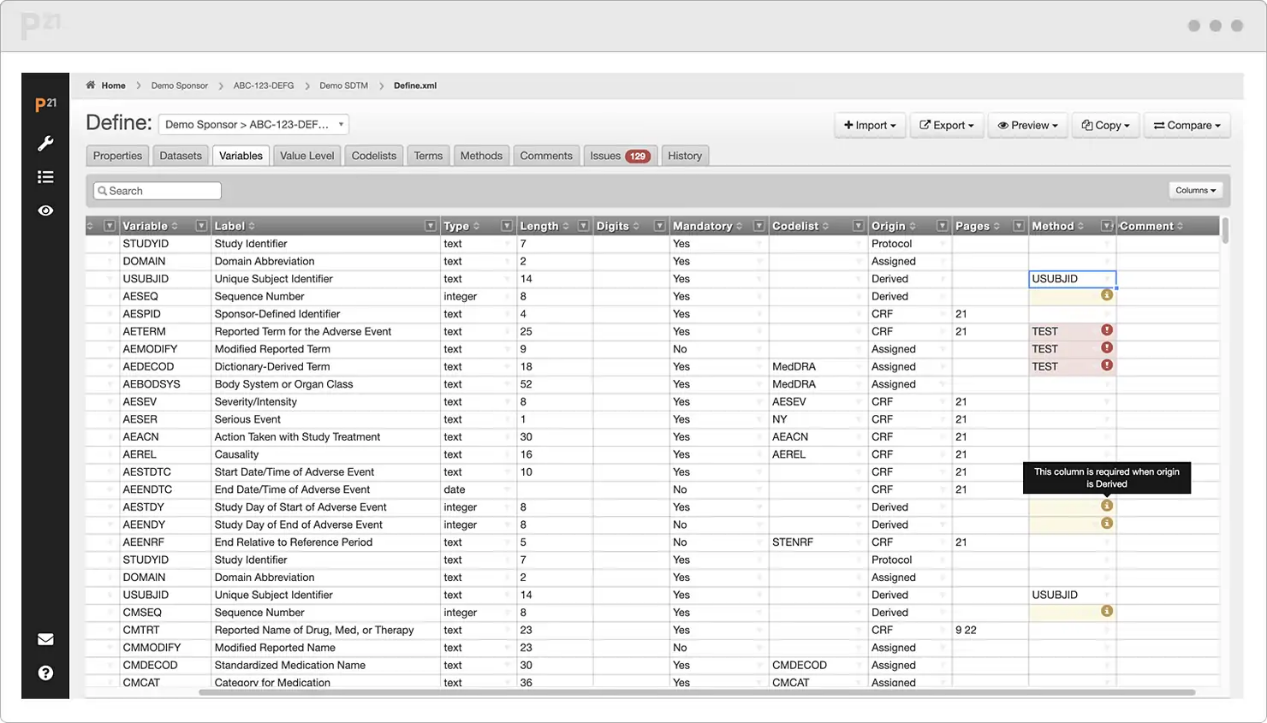
使 Define.xml 文件的准备好递交的速度提高 80%
Define.xml 文件记录了描述表格数据集结构的元数据,它告诉审阅者你的数据结构及其来源,许多递交因 Define.xml 文件错误而失败。我们的Define文件创建器会自动创建这些文件,它使您可以像电子表格一样直接管理和编辑这些文件,无需编写任何代码、XML、宏或脚本。我们的解决方案为您提供对 SDTM、SEND、ADaM 和分析结果元数据等数据集的一站式支持。您甚至可以自动填充元数据、实时验证和比较不同的版本。
如果您对该软件感兴趣,欢迎来电垂询
创腾科技:010-82676188(北京办)

(扫码询价)